La la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) finalmente dio luz verde a los a los medicamentos orales en contra de COVID-19 fabricados por las farmacéuticas Merk y Pfizer.
El presidente Andrés Manuel Lopez Obrador afirmó, en conferencia de prensa, que cuando se aprueben, van a comenzar a usarse en hospitales públicos.

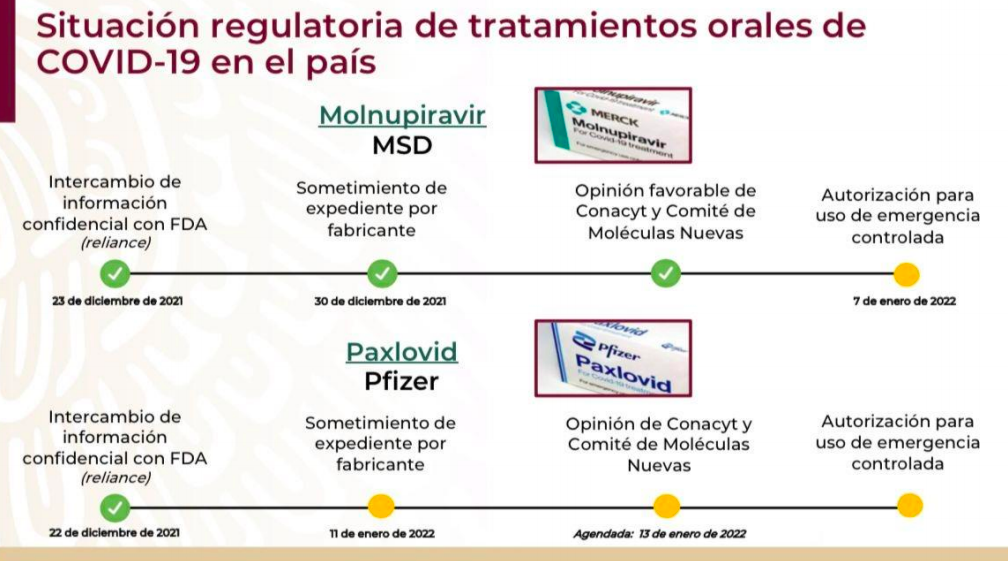
La autorización del medicamento Molnupiravir, de Merck, ya está lista, al igual que la de Pfizer este 14 de enero de 2022 Por lo mientras ya están analizando cómo se van a comprar los medicamentos y cuál será la dosis adecuada
¿Qué es el Molnupiravir?
Fue el pasado 23 de diciembre que la Administración de drogas y Alimentos de Estados Unidos autorizó el uso del medicamento molnupiravir, de la farmacéutica Merk. Este medicamento se usa para el tratamiento del coronavirus leve o moderado en adultos que son positivos al virus SARS-CoV-2 y que tienen un alto riesgo de ser graves.
Estas pastillas solo está disponibles con receta y el tratamiento debe iniciarse lo antes posible una vez que se tiene la confirmación de COVID-19, de preferencia dentro de los 5 días posteriores al inicio de síntomas. Por el momento no está autorizado para menores de 18 años porque puede afectar el crecimiento óseo y de los cartílagos.
Tampoco está autorizado para prevenir el COVID o para tratar el post COVID.

Es importante que este medicamento no sustituye la vacunación. A grandes rasgos, estas pastillas introducen “errores” en el código genético del virus que provoca el COVID para evitar que se repique.
La dosis es de 4 cápsulas de 200 miligramos por vía oral cada 12 horas durante 5 días. La Cofepris autorizó el uso de este medicamento el 7 de enero de 2022.
¿Qué es el Paxlovid?
El medicamento Paxlovid de Pfizer (tabletas de nirmatrelvir y de ritonavir envasadas en conjunto) fue autorizado en Estados Unidos el 22 de diciembre de 2021.
Está indicado para el tratamiento de la enfermedad leve a moderada en adultos y pacientes pediátricos (mayores de 12 años), que tienen un resultado positivo y que tienen un alto riesgo de desarrollar una enfermedad grave, hospitalización o muerte.
De estas pastillas, el nirmatrelvir inhibe una proteína del SARS-CoV-2 para detener su realización, mientras que el ritonavir echa paro haciendo más lenta la descomposición del nirmatrelvir.
La dosis es de tres tabletas (dos de nirmatrelvir y una de ritonavir) tomadas vía oral dos veces al día durante 5 días. La Cofepris autorizó este medicamento el 14 de enero de 2022.